 Immunizzazione passiva con VRC01 - i risultati dello studio AMP (Antibody Mediated Prevention)
Immunizzazione passiva con VRC01 - i risultati dello studio AMP (Antibody Mediated Prevention)
Alla
4th International HIV Research for Prevention Conference (HIVR4P) che si sta tenendo virtualmente in questi giorni, i ricercatori del National Institute of Allergy and Infectious Diseases (NIAID), in collaborazione con l'HIV Vaccine Trials Network (HVTN) e l'HIV Prevention Trials Network (HPTN), hanno presentato i risultati dei primi studi sull'immunizzazione passiva con un bNAb,
VRC01.
Iniziato nel 2016, quando il primo bNAB isolato dal NIAID nel 2010 è stato reso disponibile per sperimentazioni sull'uomo,
AMP si è svolto in due differenti trial,
HVTN 704/HPTN 085 e
HVTN 703/HPTN 081.
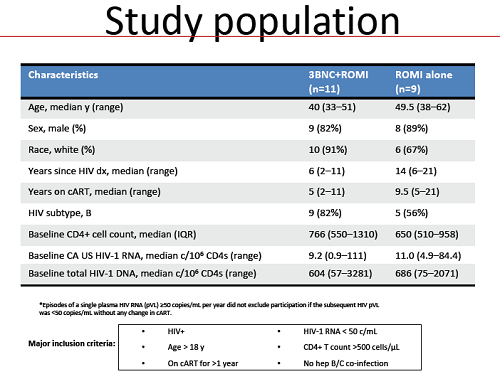
L'obiettivo era indagare se l'infusione di questo anticorpo era sicura e ben tollerata e se era in grado di proteggere dall'infezione da HIV persone ad alto rischio di infettarsi: circa 1900 donne reclutate in 7 Paesi dell'Africa Sub-sahariana (Botswana, Kenya, Malawi, Mozambico, Sud Africa, Tanzania, e Zimbabwe: dove prevale HIV-1 di sottotipo C) e circa 2400 MSM e donne transgender in Sud America (Brasile e Perù), Stati Uniti e Svizzera (dove a prevalere è l'HIV-1 di sottotipo B).
Metà dei partecipanti ha ricevuto una infusione dell'anticorpo, l'altra metà un placebo, ogni 8 settimane per 20 mesi, in tutto quindi 10 infusioni in un arco di tempo di 80 settimane (i risultati definitivi arriveranno quest'anno, i dati presentati oggi sono ancora parziali, ma alla fine le cose non cambieranno).
Due i dosaggi testati: 10 mg/kg e 30 mg/kg.
I partecipanti sono stati testati ogni 4 settimane e, se risultavano aver contratto l'infezione, il virus veniva analizzato per vedere se era suscettibile all'anticorpo.
La PrEP è stata offerta uniformemente in entrambe le sperimentazioni.
E vediamo come sono andate le cose.
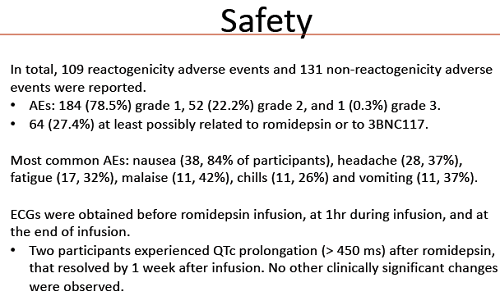
Anzitutto, come già sappiamo dai diversi studi sulla cura fatti con questo anticorpo, VRC01 è stato sicuro e ben tollerato, senza effetti avversi di rilievo.
La protezione che ha offerto dall'infezione, però, è stata deludente, perché non è stata statisticamente migliore del placebo né nel dosaggio più basso, né in quello più alto.
Quello che è emerso dai due trial è che questo bNAb in monoterapia funziona solo nelle persone che non si imbattono in un HIV che è già di suo resistente a VRC01 e che solo il 30% dei virus circolanti nei Paesi dove si è svolto lo studio sono suscettibili a questo anticorpo (e negli studi sulla cura avevamo visto con quanta facilità il virus diventi resistente a VRC01 e in genere ai bNAbs).
Le conclusioni dei ricercatori sono state che - come già abbiamo visto dai trial sulla cura - una immunizzazione con un solo anticorpo non va bene. Saranno dunque necessari studi su combinazioni di bNAbs per vedere se si ottiene una buona protezione - e sappiamo che ce ne sono di molto più potenti di VRC01.
Commento di Jon Cohen:
It has taken more than 4 years and $119 million for HIV researchers to test whether giving people infusions of antibodies made in a lab can protect them from the AIDS virus. Now, the unsatisfying answer is in: sometimes.
E sua conclusione, che condivido:
A powerful biomedical HIV prevention strategy already exists, however: a daily antiviral pill known as pre-exposure prophylaxis, or PrEP, which some AMP participants took as well. Monoclonal antibodies would have little appeal if PrEP was widely and consistently used, but many people have difficulty or don’t like taking daily pills, and its efficacy in women may be lower than men. Injected, long-acting antiretrovirals have also worked as PrEP in clinical studies but have yet to be licensed; they might provide a cheaper alternative to antibody infusions.
È vero che, finché non c'è un vaccino, tutto (o quasi) ci può andar bene, ma il ruolo che i bNAbs possono avere nella prevenzione di HIV è ancora tutto da stabilire e la competizione con la PrEP è fortissima.
FONTI: