Re: α4β7 mAB + ART: remissione virologica sostenuta in scimm
Inviato: domenica 16 ottobre 2016, 18:58
Io partecipai tanti anni fa ad una specie di studio, solo per farmi una risonanza magnetica alla testa mi diedero 70 euro 
dal 2007 informazione scientifica e community, HIV e AIDS INFO e aiuto sulla sieropositività: discutiamo di HIV e AIDS, problemi della sieropositività, farmaci e ricerca scientifica.
https://hivforum.info/forum/
Sicurissimo. Mi dispiace contraddirvi e questa regolamentazione e' valida per tutti Gli stati Che usano le GCPs ( good clinical practice) non solo per USA. Come e' scritto nel mio post "pazienti" e non volontari sani.skydrake ha scritto:Sicuro?Rob_Rob ha scritto: Pazienti nei clinical trials non possono ricevere pagamenti, e' illegale in USA.
http://forums.poz.com/index.php?topic=5 ... #msg673392

Dora ha scritto:Dora ha scritto:[...] Sia Ansari, sia Fauci, si sono affrettati a precisare che non si può dire che le scimmie siano guarite, perché si dovrà attendere di vedere che cosa accadrà in futuro.
Inoltre, non è assolutamente chiaro attraverso quale meccanismo si sia raggiunto questo controllo delle viremie. Tuttavia, i ricercatori hanno identificato una serie di correlati che, individualmente o in combinazione, possono aver contribuito al controllo:
- - la ripresa dei Th17 e Th22 (due sottogruppi di CD4);
- gli aumenti significativi di NK e altre linee cellulari che sintetizzano citochine;
- l'induzione di risposte anticorpali contro la proteina virale gp120;
- la ripresa dei livelli di acido retinoico, un derivato della vitamina A che regola le risposte immuni nell'intestino e inibisce la fibrosi.
Quello che si può dire per adesso è che il risultato ottenuto sembra davvero molto importante, al punto che Rafik Sékaly, intervistato da Jon Cohen, sostiene che questo studio "orienterà la ricerca in una direzione completamente nuova".
Sharon Lewin aggiunge che i dati presentati sono molto convincenti, ma che si dovrà vedere se saranno replicabili sull'uomo, poiché "è possibile che l'anti-α4β7 abbia funzionato perché l'impostazione dell'esperimento ha influito sul successo in un modo che potrebbe non riflettere l'infezione da HIV. Ad esempio, il team di Ansari e Fauci ha messo le scimmie sotto antiretrovirali 5 settimane dopo l'infezione, che è ben prima di quando la maggior parte delle persone iniziano la terapia".
Louis Picker insinua qualche dubbio sulla fitness dell'SIV usato per infettare i macachi: sostiene che lui ha usato lo stesso virus per poter testare il suo vaccino, ma le sue scimmie hanno avuto picchi di viremia molto più alti. Picker sospetta che qualche ignota risposta immune spieghi il controllo che le scimmie di Fauci e Ansari hanno sulle viremie dopo il trattamento. Sostiene che "quello che questo esperimento sembra fare sia dare qualche colpetto di assestamento all'equilibrio fra virus e risposta immune dell'ospite piuttosto che al virus". E dice anche di sospettare che "se prendi un anticorpo contro i CD4 e fai lo stesso esperimento potresti vedere gli stessi risultati".
Bontà sua, però, Picker ammette che nessun altro gruppo ha pubblicato finora risultati simili. Inoltre, a differenza di un anticorpo anti-CD4, l'anti-α4β7 ha un equivalente umano.
In effetti, mentre Picker è ancora lì a tergiversare da anni, il NIAID ha già iniziato 3 settimane fa ad arruolare volontari per un trial clinico: sarà un trial "esplorativo", non randomizzato, in aperto, su un singolo gruppo di pazienti, di fase I, di sicurezza/efficacia del vedolizumab su una ventina di persone con viremia soppressa dalla ART e più di 450 CD4.
Dopo le infusioni, tutti sospenderanno la ART e si vedrà che cosa accade alle viremie.
Partiamo dunque dalle considerazioni che hanno portato gli scienziati a fare questa ricerca.
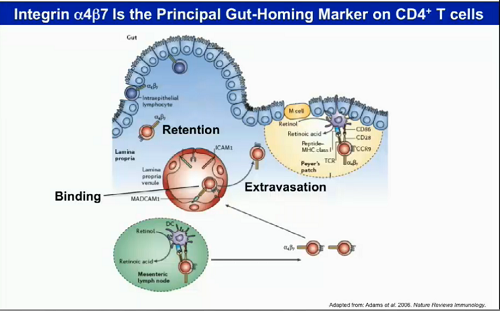
Come sappiamo, i CD4 che risiedono nel tessuto linfatico associato all'intestino (GALT) sono uno dei principali obiettivi di HIV e SIV, fin dalle fasi più iniziali dell'infezione, e la loro distruzione è parte integrante della patogenesi dell'infezione.
Queste cellule tendono ad esprimere alti livelli del recettore integrina α4β7 (α4β7hi), che usano per insediarsi nel GALT, dal momento che si lega a MAdCAM, una proteina che permette alle cellule di aderire a vene e capillari nelle pareti dell'intestino.
L'idea dei ricercatori è stata dunque di usare un anticorpo anti-α4β7 per evitare che nel GALT si insedino troppi CD4+ α4β7+ e diventino bersagli del virus.
Nel lavoro pubblicato nel 2014, l'obiettivo era di prevenire la trasmissione dell'SIV in un gruppo di macachi femmina che venivano infettate per via vaginale. Avevano dunque somministrato l'anticorpo anti-α4β7 prima di provare a infettare le scimmie e durante la fase acuta quando ormai le avevano infettate e quello che avevano visto è che le scimmie si erano, sì, infettate, ma
- 1. molto meno degli animali di controllo;
2. i CD4, sia del sangue, sia del GALT, erano stati preservati molto meglio che nei controlli;
3. il DNA provirale presente nel GALT (cioè il reservoir) era a livelli molto più bassi che negli animali non trattati.
Quindi, bloccare l'integrina α4β7 diminuiva grandemente l'infezione sia attiva, sia latente, proprio in una zona così importante come l'intestino.
Che cosa è successo, invece, nel nuovo studio? Che l'effetto protettivo del mAB α4β7 nel minimizzare la viremia nei tessuti gastrointestinali all'inizio dell'infezione ha facilitato il ripopolamento di CD4 sia nel sangue, sia soprattutto nel GALT. Questo è stato un effetto inatteso, perché i ricercatori pensavano di avere molti meno CD4 nel GALT. E non sono ancora riusciti a capire se questa ricostituzione immunitaria dipenda
- - dal controllo della viremia,
- da qualche componente del sistema immune che ha contribuito al controllo della viremia;
- da entrambe le cose.
Non è che non abbiano fatto delle ipotesi sul meccanismo (o i meccanismi) che hanno consentito alle scimmie trattate di controllare le viremie una volta sospesi tutti i trattamenti, perché - come ho scritto nel primo post - hanno osservato dei meccanismi immuni che sembrano suggerire che il controllo delle viremie sia stato immuno-mediato:
- la ripresa dei Th17 e Th22 (due sottogruppi di CD4);
- gli aumenti significativi di NK e altre linee cellulari che sintetizzano citochine;
- l'induzione di risposte anticorpali contro la proteina virale gp120;
- la ripresa dei livelli di acido retinoico, un derivato della vitamina A che regola le risposte immuni nell'intestino e inibisce la fibrosi.
Però si tratta solo di ipotesi, sulle quali ancora devono lavorare.
Lezione molto tecnica ma anche molto interessante una volta che si riesce a comprendere i meccanismi descritti. E la ricerca sembra davvero molto promettente, anche se pure in questa si va a prendere in esame situazioni di infezione acuta e non cronica. Mi piacerebbe capire quanto e come un approccio del genere, anche in caso di sperimentazione su scimmie, possa dare risultare simili.Dora ha scritto:#CROI2017 - LE MERAVIGLIE DELL'INTEGRINA α4β7
Ricordate come eravamo rimasti ad ottobre? Che gli autori principali del bel lavoro di cui parliamo in questo thread erano stupiti loro stessi dei risultati ottenuti:
Dora ha scritto:Dora ha scritto:[...] Sia Ansari, sia Fauci, si sono affrettati a precisare che non si può dire che le scimmie siano guarite, perché si dovrà attendere di vedere che cosa accadrà in futuro.
Inoltre, non è assolutamente chiaro attraverso quale meccanismo si sia raggiunto questo controllo delle viremie. Tuttavia, i ricercatori hanno identificato una serie di correlati che, individualmente o in combinazione, possono aver contribuito al controllo:
- - la ripresa dei Th17 e Th22 (due sottogruppi di CD4);
- gli aumenti significativi di NK e altre linee cellulari che sintetizzano citochine;
- l'induzione di risposte anticorpali contro la proteina virale gp120;
- la ripresa dei livelli di acido retinoico, un derivato della vitamina A che regola le risposte immuni nell'intestino e inibisce la fibrosi.
Quello che si può dire per adesso è che il risultato ottenuto sembra davvero molto importante, al punto che Rafik Sékaly, intervistato da Jon Cohen, sostiene che questo studio "orienterà la ricerca in una direzione completamente nuova".
Sharon Lewin aggiunge che i dati presentati sono molto convincenti, ma che si dovrà vedere se saranno replicabili sull'uomo, poiché "è possibile che l'anti-α4β7 abbia funzionato perché l'impostazione dell'esperimento ha influito sul successo in un modo che potrebbe non riflettere l'infezione da HIV. Ad esempio, il team di Ansari e Fauci ha messo le scimmie sotto antiretrovirali 5 settimane dopo l'infezione, che è ben prima di quando la maggior parte delle persone iniziano la terapia".
Louis Picker insinua qualche dubbio sulla fitness dell'SIV usato per infettare i macachi: sostiene che lui ha usato lo stesso virus per poter testare il suo vaccino, ma le sue scimmie hanno avuto picchi di viremia molto più alti. Picker sospetta che qualche ignota risposta immune spieghi il controllo che le scimmie di Fauci e Ansari hanno sulle viremie dopo il trattamento. Sostiene che "quello che questo esperimento sembra fare sia dare qualche colpetto di assestamento all'equilibrio fra virus e risposta immune dell'ospite piuttosto che al virus". E dice anche di sospettare che "se prendi un anticorpo contro i CD4 e fai lo stesso esperimento potresti vedere gli stessi risultati".
Bontà sua, però, Picker ammette che nessun altro gruppo ha pubblicato finora risultati simili. Inoltre, a differenza di un anticorpo anti-CD4, l'anti-α4β7 ha un equivalente umano.
In effetti, mentre Picker è ancora lì a tergiversare da anni, il NIAID ha già iniziato 3 settimane fa ad arruolare volontari per un trial clinico: sarà un trial "esplorativo", non randomizzato, in aperto, su un singolo gruppo di pazienti, di fase I, di sicurezza/efficacia del vedolizumab su una ventina di persone con viremia soppressa dalla ART e più di 450 CD4.
Dopo le infusioni, tutti sospenderanno la ART e si vedrà che cosa accade alle viremie.
Partiamo dunque dalle considerazioni che hanno portato gli scienziati a fare questa ricerca.
Come sappiamo, i CD4 che risiedono nel tessuto linfatico associato all'intestino (GALT) sono uno dei principali obiettivi di HIV e SIV, fin dalle fasi più iniziali dell'infezione, e la loro distruzione è parte integrante della patogenesi dell'infezione.
Queste cellule tendono ad esprimere alti livelli del recettore integrina α4β7 (α4β7hi), che usano per insediarsi nel GALT, dal momento che si lega a MAdCAM, una proteina che permette alle cellule di aderire a vene e capillari nelle pareti dell'intestino.
L'idea dei ricercatori è stata dunque di usare un anticorpo anti-α4β7 per evitare che nel GALT si insedino troppi CD4+ α4β7+ e diventino bersagli del virus.
Nel lavoro pubblicato nel 2014, l'obiettivo era di prevenire la trasmissione dell'SIV in un gruppo di macachi femmina che venivano infettate per via vaginale. Avevano dunque somministrato l'anticorpo anti-α4β7 prima di provare a infettare le scimmie e durante la fase acuta quando ormai le avevano infettate e quello che avevano visto è che le scimmie si erano, sì, infettate, ma
- 1. molto meno degli animali di controllo;
2. i CD4, sia del sangue, sia del GALT, erano stati preservati molto meglio che nei controlli;
3. il DNA provirale presente nel GALT (cioè il reservoir) era a livelli molto più bassi che negli animali non trattati.
Quindi, bloccare l'integrina α4β7 diminuiva grandemente l'infezione sia attiva, sia latente, proprio in una zona così importante come l'intestino.
Che cosa è successo, invece, nel nuovo studio? Che l'effetto protettivo del mAB α4β7 nel minimizzare la viremia nei tessuti gastrointestinali all'inizio dell'infezione ha facilitato il ripopolamento di CD4 sia nel sangue, sia soprattutto nel GALT. Questo è stato un effetto inatteso, perché i ricercatori pensavano di avere molti meno CD4 nel GALT. E non sono ancora riusciti a capire se questa ricostituzione immunitaria dipenda
- - dal controllo della viremia,
- da qualche componente del sistema immune che ha contribuito al controllo della viremia;
- da entrambe le cose.
Non è che non abbiano fatto delle ipotesi sul meccanismo (o i meccanismi) che hanno consentito alle scimmie trattate di controllare le viremie una volta sospesi tutti i trattamenti, perché - come ho scritto nel primo post - hanno osservato dei meccanismi immuni che sembrano suggerire che il controllo delle viremie sia stato immuno-mediato:
- la ripresa dei Th17 e Th22 (due sottogruppi di CD4);
- gli aumenti significativi di NK e altre linee cellulari che sintetizzano citochine;
- l'induzione di risposte anticorpali contro la proteina virale gp120;
- la ripresa dei livelli di acido retinoico, un derivato della vitamina A che regola le risposte immuni nell'intestino e inibisce la fibrosi.
Però si tratta solo di ipotesi, sulle quali ancora devono lavorare.
Christina Guzzo, NIH, ha presentato al CROI uno studio che è parte del grande lavoro che i ricercatori del NIAID stanno facendo attorno all'integrina α4β7. La sua lezione è stata molto tecnica, quindi cercherò di riportarne qui una breve sintesi.
VIRION INCORPORATION OF INTEGRIN α4β7: IMPLICATIONS FOR HIV-1 PATHOGENESIS
La mucosa intestinale è un sito anatomico cruciale per la replicazione di HIV e la deplezione dei CD4. Gli studi fatti dal NIAID sui macachi hanno dimostrato che, bloccando mediante un anticorpo l'integrina α4β7, che è la principale proteina che permette ai CD4 di insediarsi nella mucosa e che, quando espressa ad alti livelli, rende i CD4 un bersaglio particolarmente attraente per il virus, ne risultavano una minor trasmissione di SIV, un ritardo nella progressione della malattia e un controllo della viremia che durava per mesi anche dopo che l'anticorpo non veniva più somministrato. Il lavoro presentato al CROI mirava a capire i meccanismi che avevano consentito questo effetto protettivo dell'anticorpo anti-integrina α4β7.
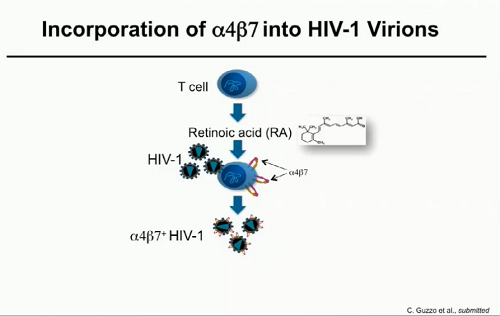
I ricercatori del NIAID hanno dunque coltivato ceppi di HIV in cellule PBMC umane, attivate in presenza e assenza di acido retinoico, poi hanno utilizzato anticorpi anti-α4β7 o anti-altri recettori cellulari per catturare i virioni e così poterli studiare.
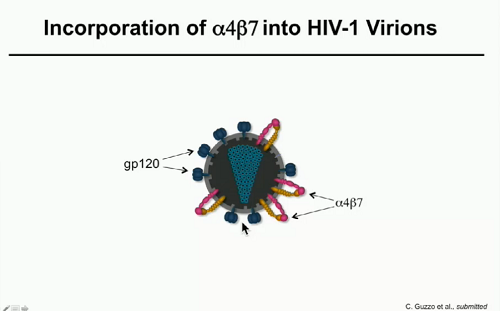
Quello che hanno osservato è quello che Christina Guzzo definisce uno slittamento di paradigma: i linfociti T sono stati attivati in modo da esprimere α4β7 sulla loro superficie, poi sono stati infettati ed è stata raccolta la progenie di questi virus e si è visto che l'integrina α4β7 era incorporata all'interno della envelope dei virioni di HIV maturi e lo era in modo funzionalmente attivo, così efficiente da aiutare il virus a infettare le cellule che esprimono la proteina MAdCAM, che a sua volta media l'infezione delle cellule circostanti.
HIV e SIV acquisiscono le loro envelope dalle membrane delle cellule da cui emergono e durante il processo catturano anche delle proteine. Quel che si è visto è che HIV emerge dalle membrane delle cellule proprio dove ci sono concentrazioni di α4β7 e così incorpora questa proteina entro la proteina Env.
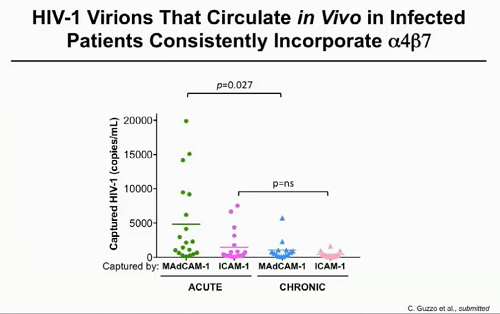
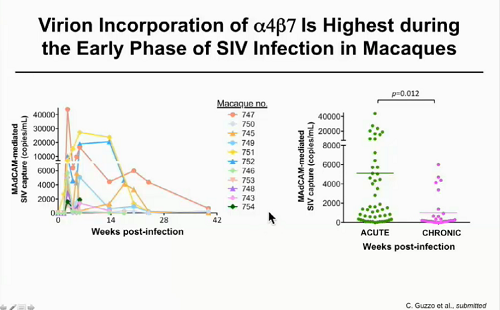
I ricercatori si sono poi chiesti se questa scoperta dell'incorporazione dell'integrina α4β7 nei virioni di HIV abbia delle implicazioni in vivo e hanno scoperto che ha una rilevanza fisiologica: i virioni presenti nelle persone non in terapia incorporano diversi livelli di questa proteina, più alti quando l'infezione è acuta, meno quando è cronica.
Nei macachi con SIV si è potuto vedere che i livelli di incorporazione della α4β7 nei virioni sono particolarmente alti quando l'infezione è nelle sue fasi iniziali.
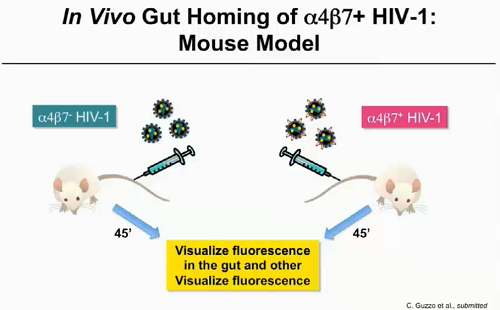
La questione affrontata a questo punto è stata quella se l'incorporazione dell'integrina α4β7 nei virioni di HIV promuova in vivo l'instaurarsi dell'infezione nell'intestino. Lo studio è stato fatto su topi umanizzati infettati con HIV che esprimeva anche la GFP (green fluorescent protein), in modo da vedere dove l'infezione si localizzasse di preferenza: dopo 45 minuti il virus iniettato era nei tessuti intestinali.
Da questo studio, si è potuto concludere che l'incorporazione di α4β7 nei virioni di HIV può promuovere il tropismo e il mantenimento del virus nei tessuti intestinali e quindi avere un impatto sia sulla trasmissione del virus, sia sulla patogenesi.
Questo consente anche di capire le ragioni per cui il trattamento con un anticorpo (il vedolizumab) che ha impedito all'integrina α4β7 di incontrarsi con il virus abbia avuto quegli effetti così protettivi che abbiamo visto nello studio sulle scimmie dell'autunno scorso.
I risultati del trial clinico su esseri umani sono attesi per l'anno prossimo.
Diciamo che questo lavoro portato al CROI è una fase intermedia, però ha dato delle informazioni che non sarà difficile confermare sul ruolo di questa proteina.rospino ha scritto:pure in questa si va a prendere in esame situazioni di infezione acuta e non cronica. Mi piacerebbe capire quanto e come un approccio del genere, anche in caso di sperimentazione su scimmie, possa dare risultare simili.
