Da notare che Silvestri porta a questo CROI molti lavori, che toccano quasi tutti gli argomenti trattati in questa lezione. Se riuscirò, almeno di qualcuno mi piacerebbe parlare qui.
Recent Advances in HIV and SIV Pathogenesis

La lezione si concentra su tre aspetti generali:
- 1) il modo in cui l’HIV distrugge la funzione immunitaria;
2) il modo in cui il sistema immunitario combatte l’HIV;
3) la patogenesi dell’HIV nell’era della terapia antiretrovirale (che è la situazione in cui si trovano attualmente la maggior parte delle persone con HIV – sempre ottimista, il nostro Guido!).

Le nostre conoscenze su come l’HIV distrugge il sistema immunitario sono molto migliorate proprio negli ultimi anni. La slide che segue è piuttosto complicata, ma descrive un modo di vedere la patogenesi dell’infezione e del danno causato dal virus.
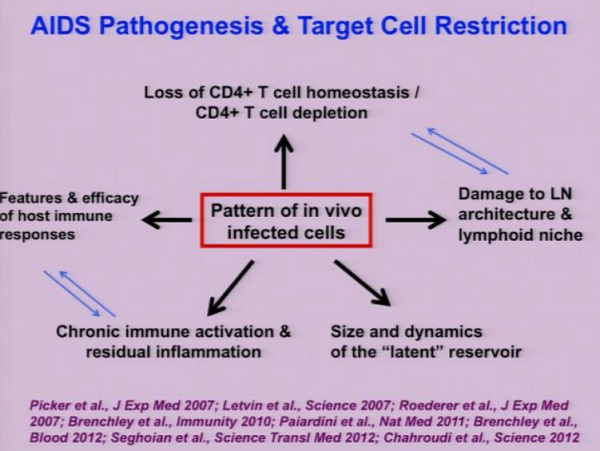
Al centro sta il modello delle cellule infette in vivo, fondamentale per comprendere se c’è progressione della malattia, perché può influenzare tanti fenomeni diversi, che sono tutti importanti nella patogenesi dell’HIV/SIV: dalla deplezione dei CD4 al danno del tessuto linfonodale, alle dimensioni del reservoir, al fenomeno della attivazione immunitaria cronica e della infiammazione residua in presenza di ART, al tipo di risposta che il sistema immunitario riesce a montare contro il virus.
Quella che segue è la descrizione di un lavoro fatto nel laboratorio di Silvestri, grazie al quale hanno dimostrato che il modello delle cellule infette in vivo è molto diverso nei casi di infezione da SIV patogenica (macachi rhesus), in cui gli animali sviluppano l’AIDS come accade in genere agli esseri umani, rispetto ai casi di infezione non patogenica (cercocebi mori), dove non c’è progressione verso l’AIDS nonostante le viremie siano alte. L’infezione dei CD4 memoria centrale è molto più alta nei macachi che nei cercocebi, e questo mostra una correlazione evidente con la progressione della malattia.
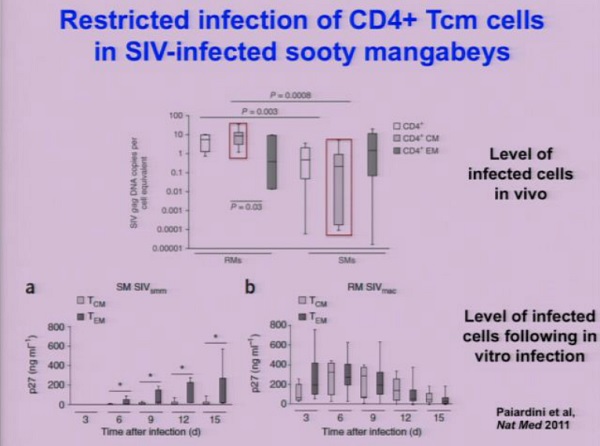
C’è infatti un sempre maggior numero di studi che dimostrano il legame fra l’infezione dei CD4 memoria centrale con la progressione della malattia anche negli esseri umani.
Pertanto, quello che la ricerca adesso deve assolutamente capire sono i fattori decisivi a livello molecolare che agiscono sul modello delle cellule infette in vivo.

Un progresso importante è stato il tentativo di risolvere il problema di capire fino a che punto l’HIV sia una malattia che distrugge i linfociti T CD4 memoria esistenti (sia attraverso l’azione diretta del virus, sia tramite l’attivazione immunitaria cronica) o se ci sia una incapacità dell’asse midollo osseo – timo di generare linfociti T naive.
Louis Picker ha sviluppato l’anno scorso un modello di deplezione dei CD4 naive nei macachi a seguito di asportazione del timo e somministrazione di anticorpi anti-CD4 e della successiva ricostruzione dei CD4. Questi animali avevano solo CD4 memoria, non avevano più CD4 naive e si è visto che avevano - in termini di viremie e numero dei CD4 una progressione della malattia simile a quella degli animali che invece avevano un timo funzionante e producevano CD4 naive.
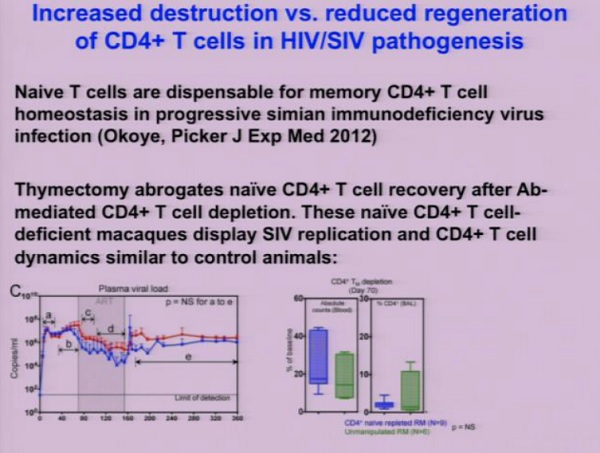
Negli ultimi anni si sono fatti dei passi avanti anche nella comprensione dei fattori di restrizione dell’ospite, che hanno un grande impatto nel contrasto della replicazione virale da parte dell’organismo e anche sulle proteine virali che, a loro volta, contrastano l’azione dei fattori di restrizione. Sono però ancora lontani dall’essere completamente capiti e si continuano a scoprire nuovi fattori di restrizione e nuove attività di restrizione. In particolare, bisogna ancora capire bene che cosa accada in vivo.

In che modo il sistema immunitario combatte l’infezione da HIV?
Nell’ultimo paio di anni sono emersi alcuni concetti nuovi, che stanno causando un mutamento di paradigma nel modo in cui guardiamo all’immunità antivirale, in particolare al ruolo dei CTL (i linfociti T citotossici), dei CD4 e dei NAb (gli anticorpi neutralizzanti).

Silvestri dedica qualche minuto ai linfociti T helper follicolari, che possono essere identificati istologicamente e funzionalmente sia negli esseri umani, sia nelle scimmie.

I Thf vengono infettati soprattutto in caso di infezione patogenica da HIV/SIV, tuttavia – paradossalmente - non subiscono una grande distruzione nei linfonodi delle persone con HIV e dei macachi con SIV e infatti, se confrontati con altri sottoinsiemi di CD4, i Thf risultano relativamente espansi, forse per dei difetti funzionali o difetti di localizzazione. Il loro ruolo nell’immunologia e nella patogenesi dell’AIDS deve essere ancora chiarito – così come non è ancora chiaro se costituiscano un reservoir di cellule latentemente infette in presenza di ART, né se la loro funzione si correli oppure no con lo sviluppo di anticorpi neutralizzanti durante la storia naturale dell’infezione.
Il ruolo dell’interferone costituisce un intero campo di studio nella comprensione della patogenesi dell’HIV/SIV e dimostra l’estrema complessità dei fenomeni biologici.

Ci sono diversi studi che ipotizzano che l’interferone possa essere un importante mediatore dell’attivazione immunitaria cronica durante le infezioni patogeniche da HIV/SIV e possa anche essere un mediatore dell’attivazione immunitaria residua in persone con viremia soppressa dalla ART.
Al tempo stesso, è ben noto che l’interferone ha potenti effetti antivirali. Quindi ha un grande potenziale nel rendere la vita difficile all’HIV e all’SIV.
È per questo, quindi, che saranno presentati al CROI diversi lavori che indagano se possa essere una buona integrazione della terapia antiretrovirale standard, altri in cui si cerca di capire se possa avere un ruolo nel distruggere i reservoir.
Nello studio descritto dalla slide seguente, fatto nel laboratorio di Silvestri, è stato somministrato interferone a dei cercocebi neri infetti da SIV, la cui infezione è caratterizzata da bassa attivazione immunitaria cronica. L’idea era quella di vedere se, dando dell’interferone, l’attivazione immunitaria aumentava e si intensificava la progressione verso l’AIDS. Quel che si è visto, però, è che – dopo un paio di mesi – non c’erano segni di peggioramento immunitario.
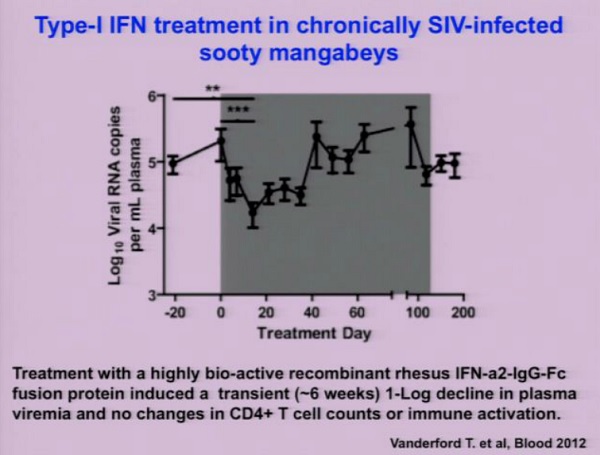
Un altro aspetto importante fra le novità sulla patogenesi riguarda l’immunologia delle mucose. È questione di grande importanza, trattata in intere sezioni del congresso, come quella che si occuperà di traslocazione microbica.
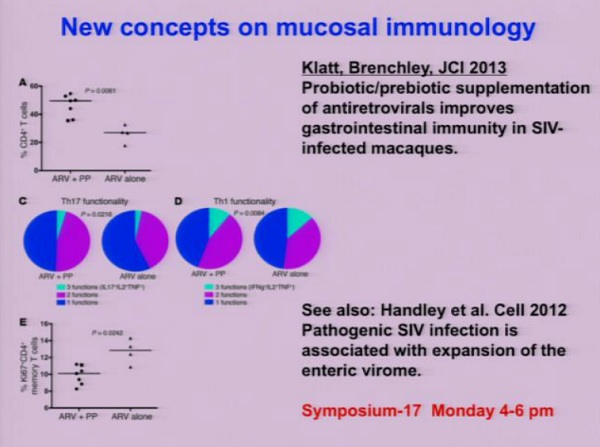
Klatt e Brenchley, per esempio, hanno appena dimostrato che la somministrazione di pro-/pre-biotici ha migliorato l’immunità gastrointestinale di macachi infetti da SIV.
La lezione di Silvestri si conclude con uno sguardo alla questione della patogenesi dell’HIV nell’era della ART, qualcosa di artificiale, che non era parte dell’evoluzione naturale dell’interazione fra ospite e virus e che ha totalmente modificato le vecchie dinamiche della patogenesi.
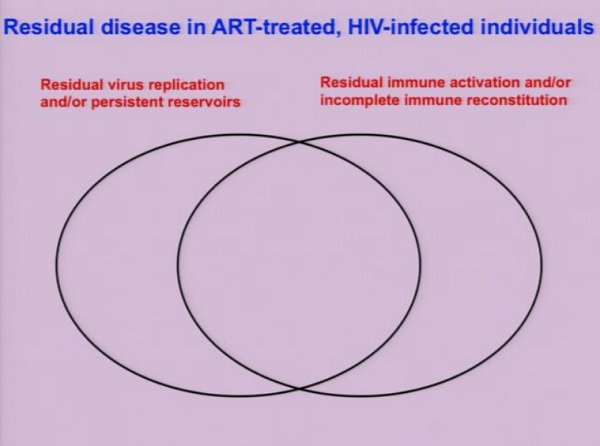
In presenza di terapia antiretrovirale, ci sono quindi due aspetti che, pur differenti, sono in parte interconnessi:
- 1) la replicazione virale residua e/o i reservoir persistenti;
2) l’attivazione immunitaria residua e/o la ricostituzione immunitaria incompleta.
Una cosa che si deve dire con chiarezza è che va bene parlare di eradicazione, ma se avessimo un modo per eliminare magicamente ogni singola copia di virus dal corpo di una persona infetta, questo non significherebbe automaticamente che quella persona sarebbe a posto da un punto di vista immunologico, perché le cicatrici inflitte al sistema immunitario dall’infezione potrebbero non essere risolte semplicemente eliminando il virus. In sostanza, potrebbe essersi creata una patologia immunitaria indipendente dal virus.
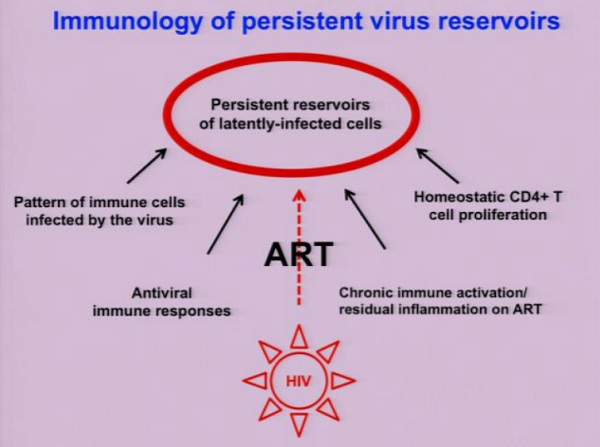
Passando ai reservoir virali persistenti, Silvestri sottolinea come la loro formazione coinvolga numerosi aspetti immunologici: dalla proliferazione omeostatica dei CD4 agli effetti dell’attivazione immunitaria cronica e della infiammazione residua sulle cellule latentemente infette, alla replicazione virale che sfugge all’azione della ART, alle risposte immuni, in particolare le reazioni CTL che possono distruggere cellule che stanno riattivando la produzione del virus, al modello delle cellule immuni infette.
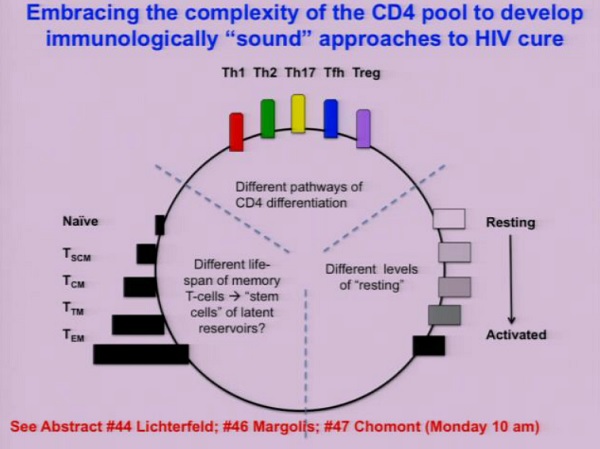
Perché si facciano dei progressi reali, è necessario che la ricerca di una cura comprenda, accetti e perfino “abbracci” l’estrema complessità del sottoinsieme dei CD4. Se non si capisce che i reservoir possono essere estremamente polimorfi, estremamente diversi da persona a persona, si rischia di dover tirare le ricerche davvero per le lunghe. Ecco perché i lavori segnalati nella slide qui sotto sono da seguire con particolare attenzione.
Quali sono le tre questioni principali da indagare?
- 1) L’identificazione di tutti i fattori (virologici e immunologici) che determinano il modello delle cellule infette in vivo durante la storia naturale dell’infezione da HIV/SIV.
2) La migliore comprensione – in vivo, nella clinica – del ruolo antivirale e/o patogenico di alcuni “poco studiati” aspetti della risposta immune dell’ospite (sappiamo molto dei CD8, ma troppo poco di Tfh, NAb, INF-I, molecole co-inibitorie, etc.).
3) La definizione dei meccanismi responsabili del formarsi (e del mantenersi durante la ART) del reservoir persistente di cellule latentemente infette.

Domanda (l’unica non troppo tecnica): negli ultimi anni 5-10 stiamo tendendo a dare la ART sempre prima, appena scopriamo l’infezione. Possiamo immaginare che, nei prossimi 5 anni, questo comporterà dei mutamenti, dei miglioramenti nella reazione immune e dunque nei rapporti fra ospite e virus, per esempio in termini di riduzione dell’attivazione immunitaria?
Risposta: ottima domanda! Vorrei proprio saperlo, se le risposte immuni saranno più efficaci.