Aggiornamento su sicurezza e tollerabilità di AGT103-T
Su
Frontiers in Medicine è uscito a metà novembre scorso
Safety and durability of AGT103-T autologous T cell therapy for HIV infection in a Phase 1 trial.
Anche se la rivista non è esattamente di prima grandezza e anche se lo studio pubblicato è abbastanza preliminare, sia perché non riferisce di tutti i pazienti arruolati, sia perché ancora non si sbilancia sull'efficacia dell'AGT103-T, dato lo stile comunicativo cui ci ha abituati l'American Gene Technologies, attendevo fanfare e cotillon. Nulla di tutto questo: né
un comunicato stampa, né una dichiarazione di Geff Galvin, solitamente ciarliero e che il 21 ottobre scorso
si limitava a ricordare che
[w]e are working to facilitate the fastest possible progression of AGT103-T, but it is not possible to predict availability yet. Neppure un tweet. Il che è strano, considerando che i risultati presentati in questo primo lavoro sono positivi.
Non ci resta, allora, che apprezzare l'estrema sobrietà della company, augurarci che quanto più il gioco si fa serio, tanto più la comunicazione si faccia misurata, e vedere l'articolo di David Pauza e colleghi, che è interessante e mi pare ben fatto.
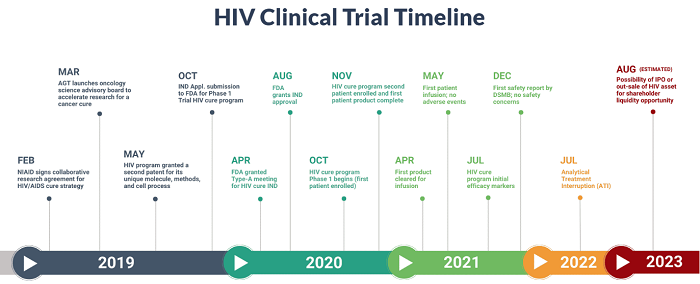
Riprendiamo brevemente il razionale della sperimentazione, perché nel corso degli anni di hype qualcosa potrebbe esser andato perduto.
Indipendentemente da forti e ben mirate risposte dei CD8, che sappiamo essere una caratteristica essenziale di un buon controllo naturale della viremia di HIV, anche avere molti CD4 Gag-specifici serve a coordinare una risposta efficace contro l'infezione. Però questi CD4 si perdono, perché proprio queste cellule sono le principali prede del virus. Quindi costituire un solido comparto di CD4 che siano da un lato Gag-specifici, e dall'altro "protetti" contro l'attacco di HIV mediante un intervento di terapia genica, è l'obiettivo dello studio di cui parliamo in questo thread.
La progettazione e la valutazione preclinica dell'AGT103-T sono state descritte in
un articolo del 2020. Qui basti dire che l'AGT103-T si compone di due parti: un vettore lentivirale, che esprime 3 microRNA che insegnano alle cellule a difendersi da HIV; e CD4 prelevati dal sangue periferico dei pazienti e in cui il sottogruppo dei CD4 Gag-specifici viene ampliato in provetta stimolando i CD4 mediante peptidi della Gag di HIV. Poi i CD4 resi resistenti al virus e Gag-specifici vengono reinfusi nel paziente e si aspetta di capire se si è riusciti a stimolare l'immunità contro il virus, controllare il carico virale e così ridurre o addirittura eliminare la necessità della terapia antiretrovirale.
La prima parte dei test sull'uomo, però, deve dimostrare che l'intervento non è tossico, che è ben tollerato, che non causa effetti avversi di rilievo.
E questo è quanto ci viene raccontato in questo articolo.
E le cose sono andate bene.
Nel
trial di fase I sono stati arruolati finora 13 partecipanti (1 sola donna), di età mediana 41 anni (26-59), valore assoluto mediano dei CD4 577 cellule/mL (473-1465), durata mediana dell'infezione 14,2 anni (3,8-28,4), durata mediana della cART 6 anni (3-24).
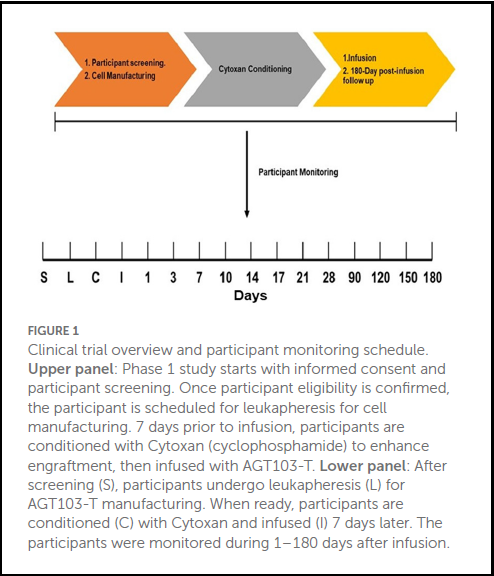
Dopo essere stati sottoposti alla procedura della leucoaferesi per raccogliere e poi modificare i CD4, circa una settimana prima della reinfusione delle loro cellule modificate i partecipanti hanno ricevuto un condizionamento con ciclofosfamide (Cytoxan), come si fa sovente nei trapianti per favorire l'attecchimento e la successiva espansione delle cellule.
Poi l'infusione: ai primi basse quantità di cellule modificate e a distanza di 45 giorni l'uno dall'altro per essere sicuri di non avere problemi immediati di sicurezza, ai successivi quantità maggiori.

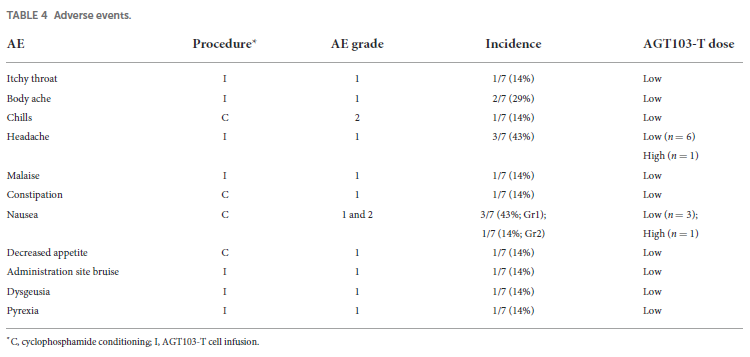
Anche se ci sono stati problemi iniziali per errori di produzione e di conservazione delle cellule modificate, l'obiettivo principale dello studio, la valutazione della sicurezza dell'AGT103-T, è stato raggiunto: tutti gli effetti avversi riportati sono stati di leggera o leggerissima entità, sono stati probabilmente connessi al condizionamento con ciclofosfamide (e ci sarà da capire con urgenza
se è davvero opportuno continuare a farlo), e si sono risolti rapidamente. Nessuna alterazione è stata rilevata a livello ematologico o biochimico.
Soprattutto, non si è verificato nessuno degli eventi più temuti nei casi di interventi con terapia genica o di ricostituzione immunitaria: non c'è stata sindrome da rilascio di citochine (
CRS), non si sono viste neurotossicità (
ICANS) o sindrome infiammatoria da ricostituzione immuntaria (
IRIS).
Tra gli obiettivi secondari, era importante valutare l'andamento generale dei leucociti, e poi quello dei linfociti e specificamente dei linfociti T e dei CD4. Non è stato osservato nulla che possa essere connesso con l'intervento, se non una diminuzione dei globuli bianchi a 3 giorni dall'infusione probabilmente dovuta agli effetti citostatici del condizionamento, poi rapidamente rientrata.
Le cellule modificate hanno avuto un picco il terzo giorno dopo l'infusione e poi sono diminuite. Ma a 180 giorni dall'infusione, che era il momento stabilito dal protocollo per concludere lo studio, ne rimanevano nel sangue ancora un buon numero, soprattutto nei due pazienti che avevano ricevuto i più alti dosaggi di CD4 modificati.
Si è osservato che l'AGT103-T ha stimolato una risposta anche nelle cellule non modificate, segnatamente nei CD8, oltre che nei CD4 non trattati. Questo è un aspetto che dovrà essere studiato nei prossimi trial.
Fino ad oggi, molte terapie geniche e cellulari sono state sperimentate per curare l'infezione da HIV e tutte si sono rivelate sicure e ben tollerate, anche se inefficaci. Quindi i risultati ottenuti da Pauza e colleghi in questo studio sono in linea con quanto abbiamo già visto in studi precedenti.
Sarà la parte della sperimentazione che indaga l'efficacia dell'AGT103-T nel favorire un controllo delle viremie a dirci se questo intervento riesce a ottenere un successo che ad altri è mancato e dunque se la ricostituzione di un comparto stabile e durevole di CD4 Gag-specifici è una strada percorribile per mantenere il controllo dell'infezione in assenza di terapia antiretrovirale.
Come sappiamo, da settembre è attivo
un trial che estende il follow up e prevede l'interruzione della cART.
Nei prossimi articoli dell'American Gene Technologies sapremo qualcosa di più. Per adesso, questo l'aggiornamento della situazione per come viene presentato
nel sito di AGT: