[CROI 2019] K. Bar: aggiornamenti sulla cura
Inviato: martedì 5 marzo 2019, 11:58
Nell'ambito del PROGRAM COMMITTEE WORKSHOP FOR NEW INVESTIGATORS AND TRAINEES, la giovanissima Katharine J Bar, University of Pennsylvania, ha avuto l'onore e l'onere di rompere una tradizione consolidata, che vedeva la lezione dedicata ad aggiornamenti sulla ricerca di una cura affidata a qualche scienziato molto esperto e sovente anche in là negli anni.
Le lezioni degli anni precedenti sono queste:
UPDATE ON HIV CURE

Nel campo ormai divenuto immenso della ricerca di una cura Bar sceglie di concentrare la sua mezz'ora di lezione su alcuni degli aspetti più innovativi.
Prima qualche questione e definizione fondamentale: perché perseguire una cura quando abbiamo una serie di combinazioni antiretrovirali estrememente efficienti nel sopprimere la viremia e impedire lo sviluppo della malattia verso l'immunosoppressione? E che cosa s'intende per cura dell'infezione da HIV?
È vero - dice Bar - la cART funziona benissimo. Ma lo stigma permane, i costi sono altissimi, l'accesso ai farmaci è difficile in molte zone del mondo, i farmaci tanto efficaci esigono ancora un prezzo in termini di tossicità e di continua aderenza. E soprattutto: la community delle persone con HIV esige una cura [questo vale nel resto del mondo, cara Katharine Bar, qui in Italia questa community mi sembra assai poco agguerrita sulla specifica questione - sarà perché da tanti anni drogata con la promessa di un vaccino da parte dell'Istituto Superiore di Sanità ...].

Quanto alle definizioni di cura, due sono i concetti basilari: 1) una cura che eradica, che richiede una radicale riduzione del reservoir, e 2) una cura funzionale, che permette una remissione prolungata, cioè un lungo controllo della viremia pur in assenza di totale distruzione del reservoir [e mi fa piacere che Bar usi la stessa potente metafora del continuo che adottai io ormai 5 anni fa - cfr. il thread ERADICAZIONE, CURA FUNZIONALE, PTC, ELITE: SOLO DEFINIZIONI?].

La principale barriera che si frappone alla cura è la persistenza di un reservoir latente, che è ben noto da tempo, ma del quale ancora sfuggono alcuni aspetti. Quello contro il quale si deve soprattutto concentrare l'attenzione è il reservoir di HIV provirale capace di replicarsi e integrato in cellule che hanno una lunga vita, sono in stato di quiescenza e riescono a persistere nonostante la cART (soprattutto CD4 memoria, ma anche macrofagi, distribuiti nel sangue e soprattutto nei tessuti linfoidi e nel sistema nervoso centrale).
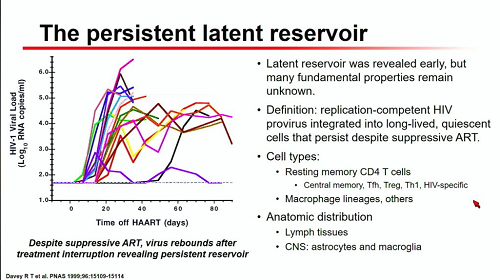
Una sfida che la ricerca sta affrontando è la misurazione del reservoir latente, perché le cellule latentemente infette contenenti virus in grado di replicarsi sono poche e facili da confondere con quelle che contengono virus difettivi, quiescenti e quindi "silenziose", distribuite in tutto il corpo e quindi difficili da individuare e raggiungere. Il classico ago nel pagliaio.

Esistono diversi modi di misurare il reservoir. Quando uno studio di qualche anno fa li ha messi a confronto, ha evidenziato il fatto che sistemi di misurazione diversi danno valori anche molto diversi e che la correlazione fra i differenti test è scarsa.
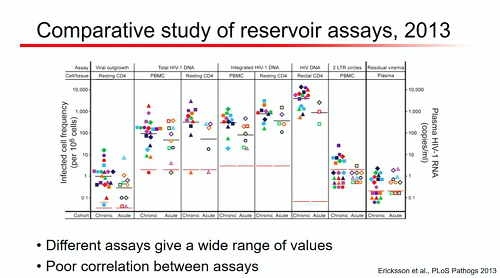
La ragione principale di queste differenze è il fatto che gran parte del provirus integrato nelle cellule è difettivo: ha grosse delezioni, è mutato così tanto dal virus wild type da aver perso la capacità di replicarsi. I metodi basati sulla PCR vedono tutto, anche i provirus difettivi.
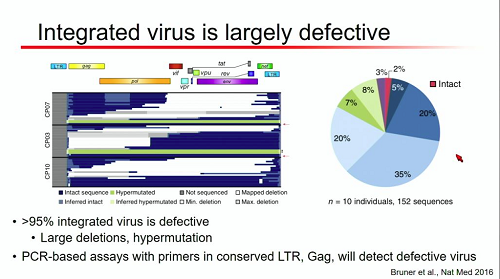
Invece, ai costosi e laboriosi metodi basati sul Viral Outgrowth Assay, che erano fino ad oggi lo standard per misurare il reservoir, sfuggono molti virus geneticamente integri che, pur non replicandosi a un primo tentativo di attivazione, mantengono intatta la loro capacità replicativa e sono pronti a replicarsi a un tentativo successivo. Il risultato è una sottovalutazione delle dimensioni effettive del reservoir.
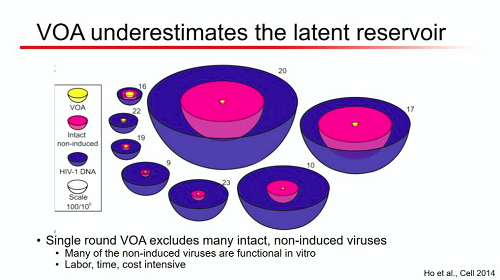
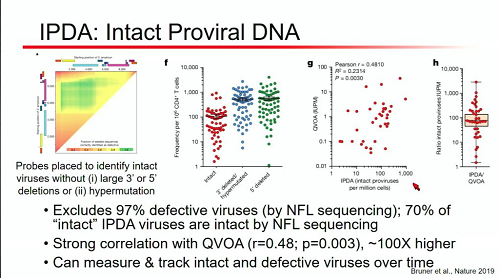
La grande novità di quest'anno, però, è l'IPDA, appena sfornato dal Siliciano Lab: un metodo per misurare il DNA provirale intatto, che è una PCR, quindi più maneggevole del VOA, con il quale si correla però in modo molto stretto, ed è in grado non solo di distinguere i provirus difettivi da quelli integri, ma anche di tracciarli nel tempo [cfr. il post UN METODO PER MISURARE IL RESERVOIR, UN METODO PER DISTINGUERE FRA I PROVIRUS DI HIV DIFETTIVI E QUELLI INTATTI].
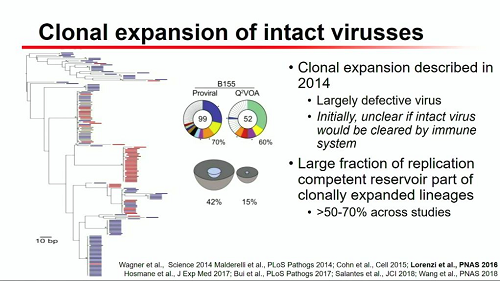
Un'altra caratteristica del reservoir latente molto importante scoperta in questi ultimi anni è l'espansione clonale del reservoir: questo, infatti, si mantiene inalterato nel tempo anche grazie alla clonazione di cellule latentemente infette contenenti provirus, che per lo più sono difettivi, ma possono anche essere intatti.
L'espansione clonale è stata descritta nel 2014 e più di recente si è dimostrato che purtroppo il sistema immunitario non è in grado di distruggere queste cellule proliferate per via clonale.
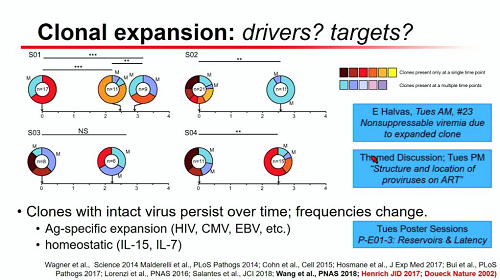
Il gruppo che fa capo a Siliciano ha mostrato che i cloni si mantengono e, mentre alcuni sono distrutti, altri si espandono nel tempo.
Una questione importante da capire, perché potrebbe fornire dei nuovi obiettivi di intervento farmacologico, è quella dei fattori che innescano l'espansione clonale. Nella parte destra della slide qui sotto sono elencate alcune presentazioni che affronteranno il problema durante il congresso.
Quando si formano i reservoir? Gli studi sulle scimmie ci dicono: molto presto, già 3 giorni dopo l'infezione e prima che si possa misurare una anche minima viremia nel sangue. Questo spiega perché anche una cART iniziata in fase acuta non è in grado di eradicare il virus.

Uno studio fatto sequenziando più volte il virus di 9 donne diversi anni prima e dopo l'inizio della terapia ha mostrato come il virus dopo anni di cART tenda ad essere molto meno differenziato, quindi ad evolversi molto meno rispetto al virus di prima della cART.
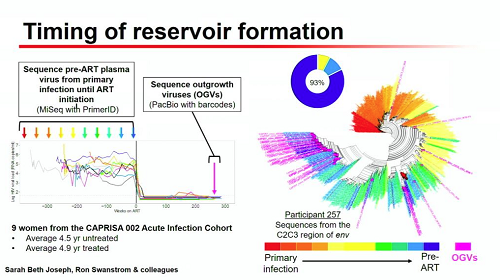
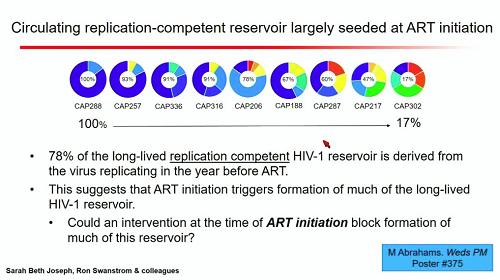
La slide successiva mostra come la maggior parte del reservoir in grado di replicarsi derivi da virus che si replicava nell'anno precedente l'inizio della cART. Questo permette di ipotizzare che con l'inizio della terapia si formi un reservoir che ha una vita molto più lunga rispetto a quello che si forma prima dei farmaci, perché si localizza in cellule che vivono più a lungo. Di qui l'ipotesi che un momento propizio per incidere sul reservoir sia proprio l'inizio della cART.
Segue la storia di Timothy Brown, fino ad ora l'unica persona curata e che nell'ultimo decennio, con il suo attivismo, è stato di ispirazione per tutta la community [e forse ora è affiancato dal London Patient - cfr. il post #CROI2019 - 12 ANNI DOPO IL BERLIN PATIENT, IL LONDON PATIENT RIAPRE LA SPERANZA DI UNA REMISSIONE A LUNGO TERMINE DELL'INFEZIONE DA HIV.]

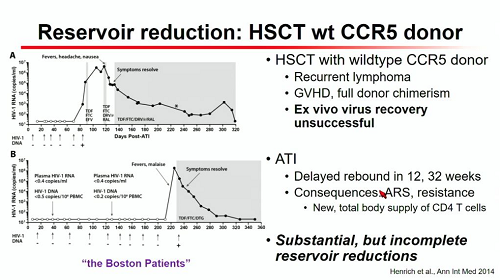
Su impulso del Berlin Patient, si è tentato di replicare il successo seguendo diverse strade: abbiamo così avuto i Boston Patients, con trapianto di staminali CCR5 positive, che hanno purtroppo avuto un rebound delle viremie dopo la sospensione della cART, ma in cui il reservoir si era ridotto in modo drastico, consentendo un periodo piuttosto prolungato di interruzione terapeutica.
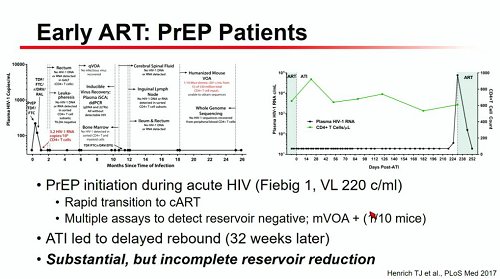
E molto interesse destano i casi di cART iniziata in fase acuta o acutissima, ad esempio in persone che hanno iniziato la PrEP senza sapere di avere da poco contratto l'infezione. Anche qui si è vista una sostanziale riduzione del reservoir. Ma ancora incompleta.
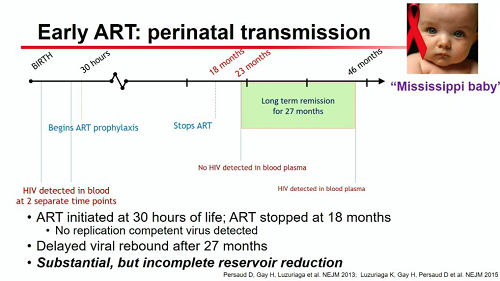
Sempre sostanziale, ma incompleta riduzione del reservoir in casi di bambini infettati attorno al momento della nascita e messi immediatamente in terapia. Il caso più famoso: quello della Mississippi Baby.
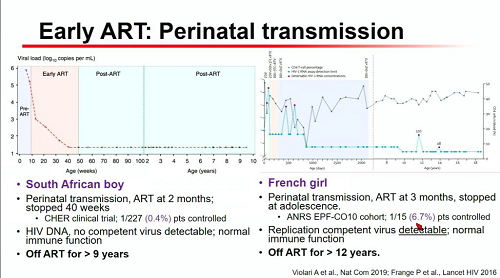
Due casi, invece, che fanno ben sperare sono quelli di un bambino sudafricano e di una ragazzina francese, che sono in sospensione della cART rispettivamente da 9 e 12 anni, con sistema immunitario normalmente funzionante e uno senza virus capace di replicazione, l'altra con virus rilevabile.
Se questo è lo stato dell'arte, come si va avanti di qui? Il punto fermo segnalato da Bar è che per ridurre il reservoir dobbiamo essere capaci di stimolare l'immunità. Alcuni lavori portati al congresso vanno proprio in questa direzione.

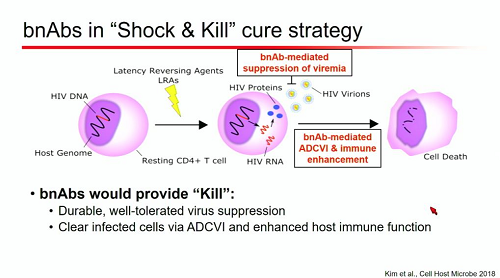
Una sintesi della strategia "shock and kill" o di "kick and kill":
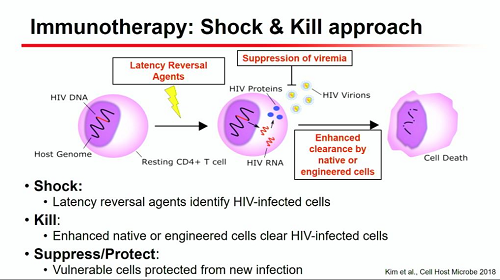
Lacomponente di "shock" o di "kick": le sostanze anti-latenza, il cui obiettivo è quello di indurre l'espressione dell'RNA virale senza al contempo attivare in modo generalizzato i linfociti T, ma riattivandone abbastanza per risvegliare il sistema immunitario, così che - grazie a opportune strategie di "killing" - sia possibile distruggere il reservoir senza che altre cellule finiscano con l'infettarsi.
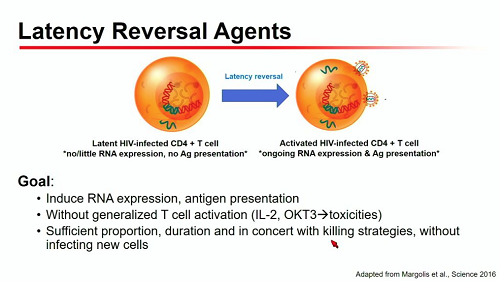
Ci sono diverse sostanze anti-latenza in sviluppo, alcune già testate per ora con risultati abbastanza deludenti, altre ancora in fase preclinica. L'idea è comunque di utilizzarne insieme più d'una, così da sfruttare diversi meccanismi di riattivazione della trascrizione virale.

La seconda componente della strategia "kick and kill" nasce dalla necessità di rendere più efficace la distruzione del reservoir mediata dai linfociti T CD8 e NK, che da soli mirano male e in modo troppo debole, e per di più sono danneggiati dalla tossicità delle sostanze anti-latenza.
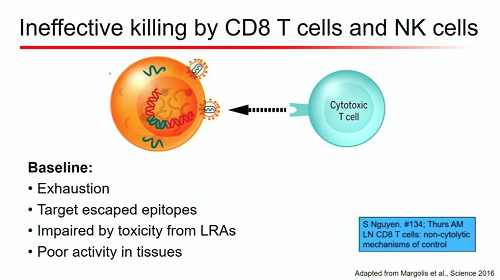
Le strategie di immunoterapia sono molte e diverse, da usarsi singolarmente o in combinazione, e sono brevemente descritte nelle slides seguenti.

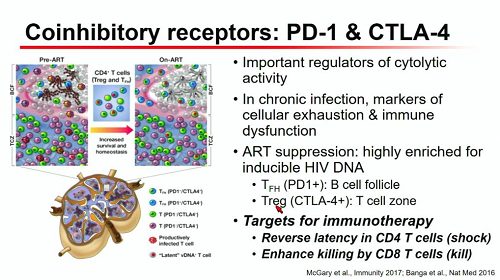

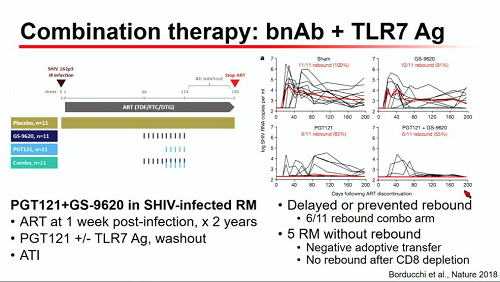
Anche gli anticorpi neutralizzanti ad ampio spettro stanno dimostrando nelle sperimentazioni cliniche di poter avere un ruolo nella cura, sia in combinazione fra loro, sia in strategie di "shock and kill" insieme a farmaci anti-latenza, sia insieme ad altri farmaci come gli agonisti del TLR-7 o 9 [poiché di tutte queste ricerche ci siamo occupati tanto in questi anni, rimando ai thread in Verso una cura].
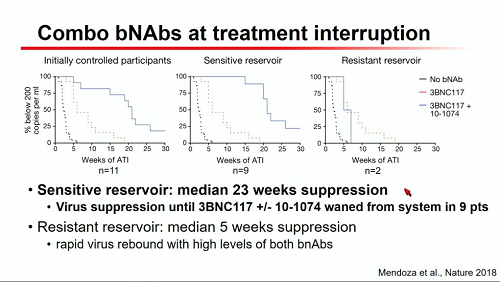
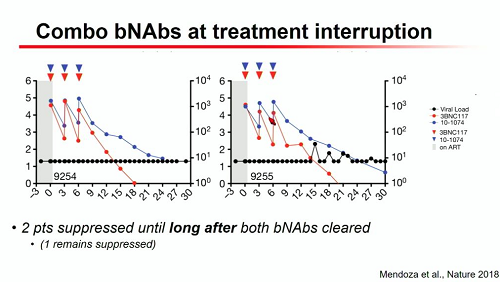

La conclusione della presentazione di Katharine Bar sintetizza la difficoltà di sciogliere gli ultimi enigmi del reservoir latente e di arrivare così ad una sua riduzione così consistente da permettere una vita senza cART. Ma ricorda anche le molte strade che la ricerca di questi anni ha aperto e sta seguendo, sottolineando come si tratti sempre di combinazioni di strategie diverse.

Le lezioni degli anni precedenti sono queste:
- [CROI 2012]J.Mellors_Reservoirs & cure research (TRAPIANTI)
[CROI 2013]M.Stevenson: Reservoir, persistenza virale e cura
[CROI 2014] La ricerca di una cura
[CROI 2015] J. Coffin: Ricerca di una cura dell’HIV
[CROI 2016] H. Günthard: Ostacoli e strategie di cura
[CROI 2017] N.Chomont_I reservoir di HIV
[CROI 2018] Günthard: progressi nella cura di HIV
UPDATE ON HIV CURE

Nel campo ormai divenuto immenso della ricerca di una cura Bar sceglie di concentrare la sua mezz'ora di lezione su alcuni degli aspetti più innovativi.
Prima qualche questione e definizione fondamentale: perché perseguire una cura quando abbiamo una serie di combinazioni antiretrovirali estrememente efficienti nel sopprimere la viremia e impedire lo sviluppo della malattia verso l'immunosoppressione? E che cosa s'intende per cura dell'infezione da HIV?
È vero - dice Bar - la cART funziona benissimo. Ma lo stigma permane, i costi sono altissimi, l'accesso ai farmaci è difficile in molte zone del mondo, i farmaci tanto efficaci esigono ancora un prezzo in termini di tossicità e di continua aderenza. E soprattutto: la community delle persone con HIV esige una cura [questo vale nel resto del mondo, cara Katharine Bar, qui in Italia questa community mi sembra assai poco agguerrita sulla specifica questione - sarà perché da tanti anni drogata con la promessa di un vaccino da parte dell'Istituto Superiore di Sanità ...].

Quanto alle definizioni di cura, due sono i concetti basilari: 1) una cura che eradica, che richiede una radicale riduzione del reservoir, e 2) una cura funzionale, che permette una remissione prolungata, cioè un lungo controllo della viremia pur in assenza di totale distruzione del reservoir [e mi fa piacere che Bar usi la stessa potente metafora del continuo che adottai io ormai 5 anni fa - cfr. il thread ERADICAZIONE, CURA FUNZIONALE, PTC, ELITE: SOLO DEFINIZIONI?].

La principale barriera che si frappone alla cura è la persistenza di un reservoir latente, che è ben noto da tempo, ma del quale ancora sfuggono alcuni aspetti. Quello contro il quale si deve soprattutto concentrare l'attenzione è il reservoir di HIV provirale capace di replicarsi e integrato in cellule che hanno una lunga vita, sono in stato di quiescenza e riescono a persistere nonostante la cART (soprattutto CD4 memoria, ma anche macrofagi, distribuiti nel sangue e soprattutto nei tessuti linfoidi e nel sistema nervoso centrale).

Una sfida che la ricerca sta affrontando è la misurazione del reservoir latente, perché le cellule latentemente infette contenenti virus in grado di replicarsi sono poche e facili da confondere con quelle che contengono virus difettivi, quiescenti e quindi "silenziose", distribuite in tutto il corpo e quindi difficili da individuare e raggiungere. Il classico ago nel pagliaio.

Esistono diversi modi di misurare il reservoir. Quando uno studio di qualche anno fa li ha messi a confronto, ha evidenziato il fatto che sistemi di misurazione diversi danno valori anche molto diversi e che la correlazione fra i differenti test è scarsa.

La ragione principale di queste differenze è il fatto che gran parte del provirus integrato nelle cellule è difettivo: ha grosse delezioni, è mutato così tanto dal virus wild type da aver perso la capacità di replicarsi. I metodi basati sulla PCR vedono tutto, anche i provirus difettivi.

Invece, ai costosi e laboriosi metodi basati sul Viral Outgrowth Assay, che erano fino ad oggi lo standard per misurare il reservoir, sfuggono molti virus geneticamente integri che, pur non replicandosi a un primo tentativo di attivazione, mantengono intatta la loro capacità replicativa e sono pronti a replicarsi a un tentativo successivo. Il risultato è una sottovalutazione delle dimensioni effettive del reservoir.

La grande novità di quest'anno, però, è l'IPDA, appena sfornato dal Siliciano Lab: un metodo per misurare il DNA provirale intatto, che è una PCR, quindi più maneggevole del VOA, con il quale si correla però in modo molto stretto, ed è in grado non solo di distinguere i provirus difettivi da quelli integri, ma anche di tracciarli nel tempo [cfr. il post UN METODO PER MISURARE IL RESERVOIR, UN METODO PER DISTINGUERE FRA I PROVIRUS DI HIV DIFETTIVI E QUELLI INTATTI].

Un'altra caratteristica del reservoir latente molto importante scoperta in questi ultimi anni è l'espansione clonale del reservoir: questo, infatti, si mantiene inalterato nel tempo anche grazie alla clonazione di cellule latentemente infette contenenti provirus, che per lo più sono difettivi, ma possono anche essere intatti.
L'espansione clonale è stata descritta nel 2014 e più di recente si è dimostrato che purtroppo il sistema immunitario non è in grado di distruggere queste cellule proliferate per via clonale.

Il gruppo che fa capo a Siliciano ha mostrato che i cloni si mantengono e, mentre alcuni sono distrutti, altri si espandono nel tempo.
Una questione importante da capire, perché potrebbe fornire dei nuovi obiettivi di intervento farmacologico, è quella dei fattori che innescano l'espansione clonale. Nella parte destra della slide qui sotto sono elencate alcune presentazioni che affronteranno il problema durante il congresso.

Quando si formano i reservoir? Gli studi sulle scimmie ci dicono: molto presto, già 3 giorni dopo l'infezione e prima che si possa misurare una anche minima viremia nel sangue. Questo spiega perché anche una cART iniziata in fase acuta non è in grado di eradicare il virus.

Uno studio fatto sequenziando più volte il virus di 9 donne diversi anni prima e dopo l'inizio della terapia ha mostrato come il virus dopo anni di cART tenda ad essere molto meno differenziato, quindi ad evolversi molto meno rispetto al virus di prima della cART.

La slide successiva mostra come la maggior parte del reservoir in grado di replicarsi derivi da virus che si replicava nell'anno precedente l'inizio della cART. Questo permette di ipotizzare che con l'inizio della terapia si formi un reservoir che ha una vita molto più lunga rispetto a quello che si forma prima dei farmaci, perché si localizza in cellule che vivono più a lungo. Di qui l'ipotesi che un momento propizio per incidere sul reservoir sia proprio l'inizio della cART.

Segue la storia di Timothy Brown, fino ad ora l'unica persona curata e che nell'ultimo decennio, con il suo attivismo, è stato di ispirazione per tutta la community [e forse ora è affiancato dal London Patient - cfr. il post #CROI2019 - 12 ANNI DOPO IL BERLIN PATIENT, IL LONDON PATIENT RIAPRE LA SPERANZA DI UNA REMISSIONE A LUNGO TERMINE DELL'INFEZIONE DA HIV.]

Su impulso del Berlin Patient, si è tentato di replicare il successo seguendo diverse strade: abbiamo così avuto i Boston Patients, con trapianto di staminali CCR5 positive, che hanno purtroppo avuto un rebound delle viremie dopo la sospensione della cART, ma in cui il reservoir si era ridotto in modo drastico, consentendo un periodo piuttosto prolungato di interruzione terapeutica.

E molto interesse destano i casi di cART iniziata in fase acuta o acutissima, ad esempio in persone che hanno iniziato la PrEP senza sapere di avere da poco contratto l'infezione. Anche qui si è vista una sostanziale riduzione del reservoir. Ma ancora incompleta.

Sempre sostanziale, ma incompleta riduzione del reservoir in casi di bambini infettati attorno al momento della nascita e messi immediatamente in terapia. Il caso più famoso: quello della Mississippi Baby.

Due casi, invece, che fanno ben sperare sono quelli di un bambino sudafricano e di una ragazzina francese, che sono in sospensione della cART rispettivamente da 9 e 12 anni, con sistema immunitario normalmente funzionante e uno senza virus capace di replicazione, l'altra con virus rilevabile.

Se questo è lo stato dell'arte, come si va avanti di qui? Il punto fermo segnalato da Bar è che per ridurre il reservoir dobbiamo essere capaci di stimolare l'immunità. Alcuni lavori portati al congresso vanno proprio in questa direzione.

Una sintesi della strategia "shock and kill" o di "kick and kill":

Lacomponente di "shock" o di "kick": le sostanze anti-latenza, il cui obiettivo è quello di indurre l'espressione dell'RNA virale senza al contempo attivare in modo generalizzato i linfociti T, ma riattivandone abbastanza per risvegliare il sistema immunitario, così che - grazie a opportune strategie di "killing" - sia possibile distruggere il reservoir senza che altre cellule finiscano con l'infettarsi.

Ci sono diverse sostanze anti-latenza in sviluppo, alcune già testate per ora con risultati abbastanza deludenti, altre ancora in fase preclinica. L'idea è comunque di utilizzarne insieme più d'una, così da sfruttare diversi meccanismi di riattivazione della trascrizione virale.

La seconda componente della strategia "kick and kill" nasce dalla necessità di rendere più efficace la distruzione del reservoir mediata dai linfociti T CD8 e NK, che da soli mirano male e in modo troppo debole, e per di più sono danneggiati dalla tossicità delle sostanze anti-latenza.

Le strategie di immunoterapia sono molte e diverse, da usarsi singolarmente o in combinazione, e sono brevemente descritte nelle slides seguenti.



Anche gli anticorpi neutralizzanti ad ampio spettro stanno dimostrando nelle sperimentazioni cliniche di poter avere un ruolo nella cura, sia in combinazione fra loro, sia in strategie di "shock and kill" insieme a farmaci anti-latenza, sia insieme ad altri farmaci come gli agonisti del TLR-7 o 9 [poiché di tutte queste ricerche ci siamo occupati tanto in questi anni, rimando ai thread in Verso una cura].





La conclusione della presentazione di Katharine Bar sintetizza la difficoltà di sciogliere gli ultimi enigmi del reservoir latente e di arrivare così ad una sua riduzione così consistente da permettere una vita senza cART. Ma ricorda anche le molte strade che la ricerca di questi anni ha aperto e sta seguendo, sottolineando come si tratti sempre di combinazioni di strategie diverse.
